Tiamina
| Substància | compost químic, medicament, ingredient culinari i medicament essencial |
|---|---|
| Massa molecular | 265,112 uma |
| Estructura química | |
| Fórmula química | C₁₂H₁₇N₄OS+ |
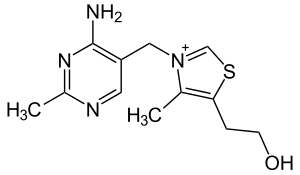 | |
SMILES canònic | Model 2D CC1=C(SC=[N+]1CC2=CN=C(N=C2N)C)CCO |
| InChI | Model 3D |
La tiamina o vitamina B1, també anomenada "tio-vitamina" (vitamina que conté sofre) és una vitamina hidrosoluble del complex B. Primerament anomenada "aneurin" degut als efectes neurològics perjudicials de la seva manca en la dieta, li va ser finalment assignat el nom genèric descriptiu de vitamina B1. Els seus derivats de fosfat estan implicats en molts processos cel·lulars. La forma més ben caracteritzada és el pirofosfat de tiamina (TPP), un coenzim en el catabolisme de sucres i aminoàcids. En els llevats, el TPP també és necessari per al primer pas de la fermentació alcohòlica.
Tots els organismes vius presenten tiamina en la seva bioquímica, però només se sintetitza en bacteris, fongs, i plantes. Els animals l'han d'obtenir de la dieta, i per això per a ells es tracta d’una vitamina. Un consum insuficient en els ocells produeix una polineuritis característica, i en els mamífers resulta en una malaltia anomenada beri-beri, que afecta el sistema nerviós perifèric (polineuritis) i/o el sistema cardiovascular, amb un resultat fatal si no era curat mitjançant l’administració de tiamina.[1] En cas de deficiència no tan severa, els senyals no específics inclouen malestar, pèrdua de pes, irritabilitat i confusió.[2]
Hi ha encara avui en dia molta feina dedicada a dilucidar els mecanismes exactes pels quals la carència de tiamina condueix als símptomes específics observats (vegeu més avall). Nous derivats de fosfat de tiamina han estat descoberts últimament,[3] cosa que emfatitza la complexitat del metabolisme de la tiamina i la necessitat de més investigació en aquest camp.
S'han descobert derivats de tiamina amb farmacocinètics millorats i s'han de considerar més eficaços en l’alleujament dels símptomes de deficiència de tiamina i en altres condicions relacionades amb la tiamina, com ara el deteriorament del metabolisme de la glucosa en la diabetis. Alguns d'aquests compostos estan representats en el següent dibuix:

Farmacocinètics importants
.
Contingut
1 Història: El descobriment de vitamines i la lesió bioquímica
2 Biosíntesi
3 Nutrició
3.1 Presència en els aliments
3.2 Referència de la ingesta diària i altes dosis
3.3 Antagonistes
4 L'absorció i el transport
4.1 Absorció
4.2 Enllaços a les proteïnes sèriques
4.3 Absorció cel·lular
4.4 La distribució tissular
4.5 Excreció
5 Les funcions dels fosfo-derivats de la tiamina
5.1 Monofosfat de tiamina
5.2 Difosfat de tiamina
5.3 Trifosfat de tiamina
5.4 Adenosina tiamina trifosfat
5.5 Adenosina tiamina difosfat
6 Deficiències
6.1 Beri-beri
6.2 Malaltia del cervell associada a l’alcoholisme
6.3 Deficiència de tiamina en aus de corral
6.4 Deficiència de tiamina en remugants
6.5 Paràlisi idiopàtica en ocells salvatges
6.6 Anàlisi i proves diagnòstiques
7 Malalties genètiques
8 Recerca
8.1 Estudis del mecanisme pel qual la deficiència de tiamina condueix a la mort neuronal selectiva
8.2 Mecanismes catalítics dels enzims dependents de ThDP
8.3 Funcions dels derivats de tiamina més enllà de la de cofactor
8.4 Carbens persistents
9 Referències
10 Enllaços externs
Història: El descobriment de vitamines i la lesió bioquímica
La tiamina va ser la primera de les vitamines solubles en aigua en ser descrita,[1] conduint, d’una banda, al descobriment de més compostos de traça essencials per a la supervivència i, de l’altra, a la idea de vitamina.
Textos mèdics xinesos ja es referien al beri-beri (una malaltia per carència de tiamina) l’any 2700 AC. No va ser fins a l’any 1884 DC. que Kanehiro Takaki (1849-1920), un general cirurgià de l'armada japonesa, va rebutjar la teoria de gèrmens prèvia i atribuí la malaltia a una dieta insuficient.[4] Canviant la dieta en vaixells d'armada, va descobrir que substituint l'arròs blanc per arròs d'ordi marró desapareixia el beri-beri (va ser sobrenomenat "Baró d'Ordi" després d’obtenir el títol nobiliari). Tanmateix, va atribuir incorrectament el benefici al consum de nitrogen, ja que la vitamina era una substància desconeguda a l'època.
L’any 1897, Christiaan Eijkman (1858-1930), un doctor militar de les Índies holandeses, descobrí que les aus de corral alimentades a partir d’una dieta basada en arròs blanc cuit desenvolupaven paràlisi, que podia ser contrarestada administrant arròs integral (amb closca).[5] Va atribuir aquest fet a un verí de nervi de l'endosperma de l’arròs, el qual no arribava al cos gràcies a la protecció de les capes exteriors del gra. Eijkman va ser guardonat amb el Premi Nobel de Medicina o Fisiologia l’any 1929, perquè les seves observacions portaren a la descoberta de les vitamines. Un company seu, Gerrit Grijns (1865-1944), va interpretar correctament la connexió entre consum excessiu d'arròs blanc i beri-beri el 1901: va concloure que l'arròs conté un nutrient essencial en les capes exteriors del gra, lògicament absent en l’arròs blanc.[6]

Estructura química de la tiamina
El 1911, Casimir Funk va aïllar una substància antineurítica de segó d'arròs que va anomenar "vitamina" (a causa de la presència d’un grup aminat). Els químics holandesos, Barend Coenraad Petrus Jansen (1884-1962) i el seu col·laborador més proper, Willem Frederik Donath (1889-1957), van aïllar i cristal·litzar l'agent actiu l’any 1926,[7] l'estructura del qual fou determinada per Robert Runnels Williams (1886-1965), químic dels EUA, el 1934. La tiamina (vitamina que conté sofre) se sintetitzà per primer cop l’any 1936 pel mateix grup.[8]
En un principi va ser anomenada “aneurin” (de vitamina antineurítica).[9] Sir Rudolph Peters, a Oxford, va presentar coloms privats de consum de tiamina com a model per entendre com una deficiència de tiamina pot conduir als símptomes fisiopatològics del beri-beri. En efecte, l’alimentació dels coloms amb arròs blanc porta a un comportament fàcilment recognoscible de retracció del cap, una condició anomenada opistòton. Si no es tracta, l'animal mor després d'uns quants dies. L'administració de tiamina durant l’etapa d'opistòton condueix a una cura completa de l'animal en tan sols 30 min. Donat que no es va observar cap modificació morfològica en el cervell del coloms abans i després del tractament amb tiamina, Peeters va introduir el concepte de lesió bioquímica.[10]
Quan Lohman i Schuster (1937) mostraren que el derivat de la tiamina difosforilada (difosfat de tiamina, ThDP) era un cofactor requerit per a la descarboxilació oxidativa del piruvat,[11] (una reacció de la qual ara és sabut que es catalitza per la piruvat deshidrogenasa), el mecanisme d'acció de la tiamina en el metabolisme cel·lular semblava ser dilucidat. Actualment, aquesta visió sembla excessivament simplificada: La piruvat deshidrogenasa és només un dels diversos enzims que requereixen el difosfat de tiamina com a cofactor; a més, altres derivats de fosfat de tiamina s'han descobert des de llavors, i també poden contribuir als símptomes observats durant la deficiència de tiamina.

Estructura tridimensional de la tiamina
Finalment, el mecanisme pel qual la fracció de tiamina del ThDP exerceix la seva funció de coenzim mitjançant la substitució del protó en la posició 2 de l'anell de tiazol va ser aclarit per Ronald Breslow l’any 1958.[12]
Biosíntesi
Les vies de biosíntesi dels complexos de tiamina ocorren en bacteris, alguns protozous, plantes i fongs.[13][14] El tiazol i les fraccions pirimidíniques se sintetitzen de forma separada per després unir-se i formar ThMP mitjançant la tiamina-fosfat sintetasa (EC 2.5.1.3). Les vies exactes poden diferir entre organismes. En E. coli i altres enterobacteriàcies el ThMP pot ser fosforilat i donar lloc al cofactor ThDP mitjançant una de tiamina-fosfat cinasa (ThMP + ATP ThDP + ADP, EC 2.7.4.16). En la majoria dels bacteris i eucariotes, el ThMP és hidrolitzat a tiamina, que llavors pot ser pirofosforilada a ThDP gràcies a l’acció la difosfocinasa de tiamina (tiamina + ATP ThDP + AMP, EC 2.7.6.2).
Les vies de biosíntesi són regulades per riboswitches en tots els organismes que sintetitzen tiamina. Si hi ha una quantitat de tiamina suficient dins la cèl·lula, la tiamina es lliga als gens de codificació de mRNA exigits en la via, evitant la traducció dels enzims. Si no hi ha presència de tiamina no té lloc la inhibició, i els enzims exigits per a la biosíntesi es produeixen. El riboswitch específic, el TPP riboswitch, és l'únic riboswitch identificat tant en organismes eucariotes com procariotes.[15]
Nutrició
Presència en els aliments
La tiamina es troba en una àmplia varietat d’aliments en quantitats reduïdes. El llevat i la carn de porc són les fonts dietètiques més importants de tiamina, en virtut de la seva ubiqüitat.
D'aquests, els cereals integrals contenen més tiamina que els grans refinats, ja que la tiamina es troba principalment en les capes externes del gra i en el germen (que s'elimina durant el procés de refinació). Per exemple, 100 g de farina de blat integral conté 0,55 mg de tiamina, mentre que 100 g de farina blanca només conté 0,06 mg de tiamina. Als EUA, la farina processada ha de ser enriquida amb mononitrat (juntament amb la niacina, ferro ferrós, riboflavina i àcid fòlic) per reemplaçar el perdut en el procés.
Alguns altres aliments rics en tiamina són la farina de civada, lli i llavors de gira-sol, arròs integral, sègol integral, els espàrrecs, les cols, la coliflor, les patates, les taronges, el fetge (de boví, porc i pollastre) i els ous.[2]
L’hidroclorur de tiamina (Betaxin) és un additiu cristal·lí higroscòpic de color blanc. S’utilitza en els aliments per donar gust caldós o de carn a salses o sopes. És un intermediari natural que resulta d'una reacció tiamina-HCl, que precedeix a la hidròlisi i la fosforilació, abans que sigui finalment emprada (en forma de TPP) en una sèrie de reaccions enzimàtiques d'aminoàcids, greixos i hidrats de carboni.[16][17]
Referència de la ingesta diària i altes dosis
La QDR en la majoria de països es troba al voltant d'1,4 mg. No obstant això, proves fetes a partir de dones voluntàries amb dosis diàries de 50 mg han mostrat un augment en l'agudesa mental.[18] No hi ha informes disponibles sobre possibles efectes adversos del consum de tiamina per excés d'ingestió d'aliments i suplements. Com que les dades són insuficients per a una avaluació quantitativa del risc, cap nivell de consum tolerable superior pot ser derivat de la tiamina.
Antagonistes
La tiamina en els aliments pot ser degradada de diverses maneres. Els sulfits, que s'afegeixen als aliments en general com a conservant,[19] ataquen la tiamina en l’estructura del pont de metilè, tallant l'anell de pirimidina de l'anell de tiazol.[2] En condicions d'acidesa la taxa d’aquesta reacció augmenta. La tiamina és degradada per thiaminases termolàbils (presents en peixos i mariscs crus).[1] Algunes thiaminases són produïdes per bacteris. Les thiaminases bacterianes són enzims de la superfície cel·lular que s’han de dissociar de la membrana abans de ser activat; la dissociació pot ocórrer en remugants en condicions d'acidosi. Els bacteris de la panxa també redueixen el sulfat a sulfit. És per això que l’alta ingesta diària de sulfat pot tenir activitats antagòniques de la tiamina.
Els antagonistes de la planta de tiamina són estables a la calor i es produeixen tant a l'orto- com al para-hydroxyphenols. Alguns exemples d'aquests antagonistes són l'àcid cafeic, l’àcid clorogènic i l'àcid tànnic. Aquests compostos interaccionen amb la tiamina per oxidar l'anell tiazol, la qual cosa el fa incapaç de ser absorbit. Dos flavonoides, quercetina i la rutina, també han estat implicats com a antagonistes de la tiamina.[2]
L'absorció i el transport
Absorció
La tiamina és alliberada per l'acció de la fosfatasa i pirofosfatasa en l'intestí prim superior. A baixes concentracions, el procés es du a terme per transport mediat i en concentracions més altes, l'absorció es produeix per difusió passiva. El transport actiu és més gran en el jejú i l'ili (que és inhibit pel consum d'alcohol i per la deficiència de fòlic).[1] Hi ha disminució en l'absorció de tiamina quan es produeix un consum diari superior a 5 mg.[20] Les cèl·lules de la mucosa intestinal tenen activitat de la tiamina pirofosfocinasa, però no està clar si l'enzim està relacionat amb l'absorció activa o no. La major part de la tiamina present en l'intestí es troba en la forma ThDP pirofosforilada, però quan arriba la tiamina en la part serosa de l'intestí ho fa sovint de forma lliure. L'absorció de la tiamina per la cèl·lula de la mucosa està probablement relacionat d'alguna manera amb la seva fosforilació / desfosforilació. A la part serosa de l'intestí, s’ha demostrat que la descàrrega de la vitamina per aquestes cèl·lules és dependent de Na+ - dependent ATPasa.[2]
Enllaços a les proteïnes sèriques
La majoria de la tiamina en el sèrum està unida a proteïnes, principalment a l'albúmina. Aproximadament el 90% del total de tiamina en sang es troba en els eritròcits. Una unió a proteïnes específiques anomenades proteïnes d'unió a la tiamina (TBP) s'ha identificat en el sèrum de rata i es creu que és una proteïna transportadora regulada per hormones, que és important per a la distribució de la tiamina en els teixits.[2]
Absorció cel·lular
L’absorció de tiamina per les cèl·lules de la sang i altres teixits es produeix per mitjà de transport actiu i difusió passiva.[1] Al voltant del 80% de la tiamina intracel·lular és fosforilada i la majoria s'uneix a proteïnes. En alguns teixits, l'absorció de la tiamina i la secreció sembla estar mediat per un transportador de tiamina soluble que és dependent de Na + i un gradient de protons transcelular.[2]
La distribució tissular
L'emmagatzematge de tiamina en humans és de 25 a 30 mg amb les majors concentracions en el múscul esquelètic, cor, cervell, fetge i ronyons. El ThMP i la tiamina lliure (no fosforilada) és present en el plasma, la llet, el líquid cefaloraquidi i en gairebé tots els fluids extracel·lulars. A diferència de les formes altament fosforilats de la tiamina, el ThMP i la tiamina lliures són capaços de travessar les membranes cel·lulars. El contingut de tiamina en els teixits humans són menors que els d'altres espècies.[2][21]
Excreció
La tiamina i els seus metabòlits (àcid carboxílic 2-metil-4-amino-5-pirimidina, àcid 4-metil-tiazol-5-acètic i àcid acètic tiamina) s’excreten principalment en l'orina.[22]
Les funcions dels fosfo-derivats de la tiamina
La Tiamina és, principalment, la forma de transport de la vitamina mentre que les formes actives són les formes fosforilades derivades de la tiamina. Es coneixen cinc derivats naturals de la fosfotiamina: el monofosfat de tiamina (ThMP), el difosfat de tiamina (thDP) anomenat molt sovint pirofosfat de tiamina (TPP), el trifosfat de tiamina (ThTP) i recentment descoberts l’adenosina tiamina trifosfat (AThTP) i l’adenosina tiamina difosfat (AThDP).
Monofosfat de tiamina
No es coneix cap funció fisiològica del ThMP.
Difosfat de tiamina
La síntesi del difosfat de tiamina (ThDP), també coneguda com a pirofosfat de tiamina (TPP) o cocarboxilasa, és catalitzada per un enzim anomenat tiamina difosfocinasa a partir de la reacció següent:
Tiamina + ATP → TPP + AMP ( enzim catalitzador: 2.7.6.2 )
El TPP és un coenzim de molts enzims que catalitzen la transferència d'unitats de dos àtoms de carboni i en particular la deshidrogenació (descarboxilació i subsegüent conjugació amb el coenzim A) de 2-oxoàcids (α-cetoàcids). A tall d’exemples destaquen els següents enzims:
- Presents en moltes espècies:
- La piruvat deshidrogenasa i el 2-oxoglutarat deshidrogenasa (α-cetoglutarat deshidrogenasa.
- Cadena bifurcada d’α-cetoàcid dehidrogenasa
- 2-hidroxiphytanoyl-CoA liasa
- Transcetolasa
- Present en algunes espècies:
- Piruvat descarboxilasa (en llevats)
- En enzims bacterians addicionals
Els enzims trancetolasa, piruvat deshidrogenasa (PDH) i el 2-oxoglutarat deshidrogenasa (OGDH) tenen importància en el metabolisme dels glúcids. La trancetolasa és un enzim citosòlic que té un paper clau en la via de les pentoses fosfat. Aquesta ruta és essencial per a la biosíntesi de les pentoses ribosa i desoxiribosa. El PDH mitocondrial i l’OGDH són catalitzadors de metabòlits relacionats amb la biosíntesi de l’adenosina trifosfat (ATP), la forma més important de transport d’energia a la cèl·lula. El PDH connecta la glicòlisi amb el cilce de Krebs (també anomenat cicle de l’àcid cítric) mentre que la reacció catalitzada pel OGDH és un pas restringit dins del cicle de Krebs perquè necessitat una quantitat d’energia elevada per iniciar-se. A nivell del sistema nerviós, el PDH també està implicat en la producció d’acetilcolina (neurotransmissor) i en la biosíntesi de mielina.[23]
Trifosfat de tiamina
El trifosfat de tiamina (ThTP) ha estat considerat durant molt temps una forma de la tiamina específica de l’activitat neuronal. Tanmateix, recentment s’ha demostrat que la ThTP existeix en bacteris, fongs, plantes i animals que fan pensar que la ThTP té un paper més molt més general dins de la cèl·lula.[24] En particular a l’Escherichia coli, sembla que té un paper en resposta a la inanició dels aminoàcids.[25]
Adenosina tiamina trifosfat
L’Adenosina tiamina trifosfat (AThTP) s’ha descobert recentment en l’Escherichia coli ion s’acumula com a resultat de la inanició del carboni.[3] A l’E. Coli, l’AThTP podria representar fins a un 20% de la tiamina total. També existeix en menors quantitats als llevats, arrels de les plantes i en teixits animals.[26]
Adenosina tiamina difosfat
L’Adenosina tiamina difosfat (AThDP) existeix en quantitats petites al fetge dels vertebrats. Tanmateix, encara es desconeix la seva funció.[26]
Deficiències
Els derivats de la tiamina i els enzims que en depenen, estan presents a totes les cèl·lules del cos, per tant, una deficiència de tiamina semblaria afectar adversament tots els sistemes d’òrgans. Tot i això, el sistema nerviós i el cor són particularment sensibles a una deficiència de tiamina, a causa del seu metabolisme altament oxidatiu.
La deficiència de tiamina pot conduir a una fatiga severa dels ulls i problemes importants com ara la neurodegeneració, el desgast i la mort. La manca de tiamina pot ser causada per una malnutrició, una dieta alta en aliments rics en tiaminasa (peix cru d’aigua dolça, mariscs crus, falgueres) i/o aliments rics en factors anti-tiamina (te, cafè, nous de betel),[27] i per greus estats de desnutrició associats a malalties cròniques, com l’alcoholisme, les malalties gastrointestinals, VIH-SIDA, i vòmits persistents.[28] Es creu que moltes persones amb diabetis tenen una deficiència de tiamina i que això pot estar relacionat amb algunes de les complicacions que poden ocórrer.[29][30]
Algunes de les síndromes conegudes causades per la deficiència de tiamina són: el beri-beri i la síndrome de Wernicke-Korsakoff, malalties també associades amb l’alcoholisme crònic.
Beri-beri
El beri-beri és una malaltia neurològica i cardiovascular. Les tres formes principals del trastorn són: el beri-beri sec, el beri-beri humit, i el beri-beri infantil.[22]
Beri-beri sec: està principalment caracteritzat per la neuropatia perifèrica, que consisteix en el deteriorament de la simetria de les funcions sensorials, motores i reflexes, afectant bàsicament les extremitats i causant flonjor de bessons.[28]
Beri-beri humit: està associat amb la confusió mental, el desgast muscular, l’edema, la taquicàrdia, la cardiomiàlgia, i amb la insuficiència cardíaca congestiva a més de la neuropatia perifèrica.[1]
Beri-beri infantil: apareix en nadons alletats per mares amb dèficit de tiamina (les quals poden no mostrar cap signe de deficiència de tiamina). Els nadons poden manifestar les formes cardíaca, afònica o pseudomeningítica de la malaltia. Els nadons amb beri-beri cardíac sovint presenten plors forts i penetrants, vòmits i taquicàrdia.[22] Convulsions are not uncommon, and death may ensue if thiamine is not administered promptly.[28] Les convulsions no són infreqüents, i es pot produir la mort si no s’administra tiamina ràpidament.
Durant el tractament amb tiamina es produeix una ràpida millora, en general, al cap de 24 hores.[22] Les millores de la neuropatia perifèrica poden requerir diversos mesos de tractament amb tiamina.[31]
Malaltia del cervell associada a l’alcoholisme
Les cèl·lules del sistema nerviós i altres cèl·lules de suport (com les cèl·lules glials) del sistema nerviós, requereixen tiamina. Alguns exemples de trastorns neurològics que estan associats a l’abús de l’alcohol inclouen l’encefalopatia de Wernicke (WE, síndrome de Wernicke-Korsakoff) i la psicosi de Korsakoff (trastorns amnèsics) així com diferents graus de discapacitat cognitiva.[32]
L'encefalopatia de Wernicke és la manifestació més freqüent de deficiència de tiamina en la societat occidental,[33] tot i que també pot donar-se en pacients amb deficiències nutricionals provocades per altres causes, com la gastroenteritis,[33] la VIH-SIDA, i l’administració imprudent de glucosa per via parenteral o per hiperalimentació sense l’adequada complementació de vitamina B.[34] Aquest és un sorprenent trastorn neuropsiquiàtric caracteritzat per la paràlisi dels moviments oculars, per la postura i marxa anormals, i per considerables trastorns de les funcions mentals.[35]
Els alcohòlics poden presentar deficiència de tiamina per les següents causes:
- Consum nutricional inadequat: els alcohòlics tendeixen a ingerir menys quantitat de tiamina de la que està recomanada.
- Disminució de l’absorció de tiamina al tracte gastrointestinal. En l’aguda exposició a l’alcohol, el transport actiu de tiamina als enteròcits és pertorbat.
- Disminució de les reserves hepàtiques de tiamina a causa de l’esteatosis hepàtica o fibrosis.[36]
- Deficiències en l’ús de tiamina: el magnesi, el qual és requerit en la unió de tiamina als enzims que la necessiten dins al cèl·lula, també és deficient a causa de la consumició crònica d’alcohol. L’ús ineficient de qualsevol tiamina que arriba a les cèl·lules agreujarà encara més la deficiència de tiamina.
- L’etanol per se inhibeix el transport de la tiamina en el sistema gastrointestinal i bloqueja la fosforilació de la tiamina al seu cofactor (ThDP).[37]
La Psicosi de Korsakoff es considera que, en general, té lloc amb el deteriorament de la funció cerebral en pacients amb diagnòstic inicial de WE.[38] Aquesta és una síndrome caracteritzada per amnèsia retrògrada i anterògrada, deteriorament de les funcions conceptuals i disminució de l’espontaneïtat i la iniciativa.[28]
Després d’una millora en la nutrició i de l’eliminació del consum d’alcohol, alguns deterioraments relacionats amb la deficiència de tiamina s’inverteixen; en particular, el baix funcionament cerebral, tot i que en casos més greus, la síndrome de Wernicke-Korsakoff deixa danys permanents.
Deficiència de tiamina en aus de corral
Com que la majoria dels pinsos utilitzats en les dietes d'aus de corral contenen quantitats suficients de vitamines per satisfer les necessitats d'aquesta espècie, les deficiències en aquesta vitamina no es produeixen en dietes comercials. Aquesta era, si més no, l'opinió en la dècada de 1960.[39]
Els pollastres adults mostren signes tres setmanes després d’haver estat alimentats amb una dieta deficient. En els pollastres joves, els signes poden aparèixer abans de les 2 setmanes d'edat.
L’inici és sobtat en pollastres joves. Apareix anorèxia i una manera inestable de caminar. Més tard, apareixen signes locomotors, començant amb una paràlisi aparent dels músculs flexors dels dits dels peus. La posició característica s’anomena “observant les estrelles”, és a dir, una gallina asseguda sobre les seves sofrages i el cap en posició d’opistòton.
La resposta a l’administració de la vitamina és bastant ràpida, unes poques hores després d’aquesta.[40][41]
Els diagnòstics diferencials inclouen la deficiència de riboflavina i l’encefalomielitis aviar. En la deficiència de riboflavina, els “dits dels peus ondulats” són un símptoma característic. El tremolor muscular és típic de l’encefalomielitis aviar. Un diagnòstic terapèutic pot ser probat per suplements de tiamina únicament en l’ocell afectat. Si els animals no responen en poques hores, la deficiència de tiamina pot ser descartada.
Deficiència de tiamina en remugants
La polioencefalomalàcia (PEM) és el trastorn per deficiència de tiamina més comú en animals joves remugants i noregumants. Els símptomes del PEM inclouen una intensa, però transitòria, diarrea, llanguiment, moviments circulars, observar les estrelles o opistòton (cap tirat enrere sobre el coll), i tremolors musculars.[42] La causa més comuna és una alimentació alta en carbohidrats, que conduiex a la proliferació de bacteris productors de la tiaminasa; tot i que la ingesta de tiaminasa sintètica (per exemple, en la falguera mascle), o la inhibició de l’absorció de la tiamina per una alta ingesta de sofre, també són possibles.[43] Una altra causa de PEM és la infecció per Clostridium sporogenes o Bacillus aneurinolyticus. Aquests bacteris produeixen tiaminases, que causaran una deficiència aguda de tiamina en l’animal afectat.[44]
Paràlisi idiopàtica en ocells salvatges
Últimament, la deficiència de tiamina ha estat identificada com a causa de la malaltia paralitzadora que afecta als ocells salvatges de l’àrea del mar Bàltic, descoberta l’any 1982.[45] En aquest cas, existeixen dificultats per a mantenir les ales plegades al costat del cos en repòs, pèrdua de l’habilitat de volar i en la veu, amb paràlisis eventuals de les ales, cames i la mort. Afecta principalment ocells de 0.5-1 kg com el gavià argentat de potes roses (Larus argentatus), l’estornell vulgar (Sturnus vulgaris) i l’èider comú (Somateria mollissima). Algunes investigacions han assenyalat que, “Atès que les espècies investigades ocupen una gran varietat de nínxols ecològics i posicions en la cadena alimentària, estem oberts a la possibilitat que altres classes d'animals puguin patir també la deficiència de tiamina.”[45]p. 12006
Anàlisi i proves diagnòstiques
Una prova de diagnòstic positiva per a la deficiència de tiamina pot ser determinada mesurant l’activitat de l’enzim transcetolasa en els eritròcits (Assaig d’Activació de la Transcetolasa Eritrocítica). La tiamina, així com els seus derivats fosfats, també pot ser detectada directament a la sang, als teixits, als aliments, als pinsos i als productes farmacèutics després de la conversió de la tiamina en derivats dels tiocroms fluorescents (Assaig del Tiomcrom) i separació per cromatografia líquida d’alt rendiment (HPLC).[46][47][48] En informes recents han sorgit, com a tècniques alternatives per a la determinació i seguiment de la tiamina en mostres, una sèrie de tècniques d’Electroforesis Capil·lars (EC) i reaccions enzimàtiques dins els capil·lars.[49]
Malalties genètiques
Les malalties genètiques que afecten al transport de tiamina són rares i poc freqüents però serioses i greus. L’anèmia megaloblàstica responsiva a la tiamina (TRMA) i combinada amb diabetis mellitus i deficiència auditiva sensorineural[50] és una malaltia autosòmica recessiva causada per mutacions al gen SLC19A2,[51] que codifica per un transportador de tiamina d’alta afinitat. Els pacients de TRMA no tenen signes de deficiència sistemàtica de tiamina, suggerint que es deu tractar d’una desocupació en el sistema de transport de tiamina. Això ha conduït el descobriment d’un segon centre transportador de tiamina d’alta afinitat codificat pel gen SLC19A3.[52][53] La síndrome de Leigh (SNEM) és un trastorn neurodegeneratiu heretat i progressiu que afecta principalment a nens durant els primers anys de vida. Les similituds patològiques entre la síndrome de Leigh i el WE ens ha portat a la hipòtesi on la causa és un defecte en el metabolisme de la tiamina i no en la concentració. Un dels descobriments és per ara l’anormalitat trobada en l’activació del complex PDH.[54]
Altres malalties on està implicada la funció i el rol de la tiamina són: la SNEM, una síndrome paraneoplàsica i l’atàxia estacional Nigeriana. A més, alguns trastorns heretats d’enzims dependents de ThDP han estat trobats,[55] possiblement com a resposta al tractament de tiamina.[28]
Recerca
La recerca en aquest camp, principalment, està centrada en els mecanismes pels quals la deficiència de tiamina condueix a una mort neuronal en relació amb la psicosi de Wernkicke Korsakoff. Un altre camp de recerca important és el que s’ocupa de l’estudi molecular per entendre, a aquest nivell, els mecanismes implicats en la catàlisi de ThDH. Recentment, la investigació també ha estat focalitzada en l’estudi i la comprensió dels papers i funcions a més dels de cofactors d’alguns d’altres derivats com la ThTP o la ATHTP.
Estudis del mecanisme pel qual la deficiència de tiamina condueix a la mort neuronal selectiva
Experimentalment, la inducció del beri-beri amb mielopatia a pollastres pot ser un bon model per estudiar aquestes formes de mielopatia en vista de diagnòstics i tractaments.[56] A partir d’estudis que utilitzen models de rata, s’ha observat una relació entre la deficiència de tiamina i una carcinogènesi de còlon.[57] El model de rates també s’utilitza en la investigació d’encefalopaties de Wernicke.[58] Els ratolins amb carència de tiamina són un clàssic model d’estrès oxidatiu sistemàtic molt utilitzat en la recerca de la malaltia de l’Alzheimer.[59]
Mecanismes catalítics dels enzims dependents de ThDP
Molts estudis estan centrats a entendre la interacció entre la ThDP i els enzims dependrents de ThDP a la catàlisi.[60][61]
Funcions dels derivats de tiamina més enllà de la de cofactor
Existeixen altres compostos de tiamina am és del ThDH en la majoria de cèlules de molts organismes, incloent-hi bacteris, fongs, plantes i animals. Entre aquests compostos estan el trifosfat de tiamina (ThTP) i el trifosfat d’adenosina (AThTP) dels quals es pensa que tenen papers més enllà del de cofactor. Tanmateix, fins al moment, es desconeix en quina mesura hi participen a nivell de símptomes.[3][26][62][63]
Carbens persistents
La producció d'1,2-di(furan-2-yl)-2-hydroxyethanone a partir del furfural està catalitzada per tiamina a través d’un carben (molècula que conté parells d’electrons de valència lliures del centre carboni) relativament estables. Aquesta reacció, estudiada el 1957 per R.Breslow, va ser la primera evidència de l’existència de carbens persistents.
Referències
↑ 1,01,11,21,31,41,5 Mahan LK, Escott-Stump S, editors. Krause's food, nutrition, & diet therapy. 10th ed. Philadelphia: W.B. Saunders Company; 2000
↑ 2,02,12,22,32,42,52,62,7 Combs, G. F. Jr. The vitamins: Fundamental Aspects in Nutrition and Health. 3rd Edition. Ithaca, NY: Elsevier Academic Press; 2008
↑ 3,03,13,2 Bettendorff L, Wirtzfeld B, Makarchikov AF, Mazzucchelli G, Frédérich M, Gigliobianco T, Gangolf M, De Pauw E, Angenot L and Wins P «Discovery of a natural thiamine adenine nucleotide». Nature Chem. Biol., 3, 2007, pàg. 211–212. DOI: 10.1038/nchembio867.
↑ McCollum EV. A History of Nutrition. Cambridge, MA: Riverside Press, Houghton Mifflin; 1957.
↑ Eijkman, C. (1897). Eine Beriberiähnliche Krankheit der Hühner. Virchows Arch. Pathol. Anat. 148: 523.
↑ Grijns, G. (1901) Over polyneuritis gallinarum. I. Geneesk. Tijdscht. Ned. Ind. 43, 3-110
↑ Jansen, B.C.P. and Donath, W.F. (1926) On the isolation of antiberiberi vitamin. Proc. Kon. Ned. Akad. Wet. 29: 1390-1400.
↑ Williams, R.R. and Cline, J.K. (1936). Synthesis of vitamin B1. J. Am. Chem. Soc. 58: 1504-1505.
↑ Carpenter KJ. Beriberi, white rice, and vitamin B: a disease, a cause, and a cure. Berkeley, CA: University of California Press; 2000
↑ Peters, R.A. (1936). The biochemical lesion in vitamin B1 deficiency. Application of modern biochemical analysis in its diagnosis. Lancet 1: 1161-1164.
↑ Lohmann, K. and Schuster, P. (1937). Untersuchungen über die Cocarboxylase. Biochem. Z. 294, 188-214.
↑ Breslow R «On the mechanism of thiamine action. IV.1 Evidence from studies on model systems». J Am Chem Soc, 80, 1958, pàg. 3719–3726. DOI: 10.1021/ja01547a064.
↑ Webb ME, Marquet A, Mendel RR, Rebeille F & Smith AG (2007) Elucidating biosynthetic pathways for vitamins and cofactors. Nat Prod Rep 24, 988-1008.
↑ Begley TP, Chatterjee A, Hanes JW, Hazra A & Ealick SE (2008) Cofactor biosynthesis—still yielding fascinating new biological chemistry. Curr Opin Chem Biol 12, 118-125.
↑ Switching the light on plant riboswitches. Samuel Bocobza and Asaph Aharoni Trends in Plant Science Volume 13, Issue 10, October 2008, Pages 526-533 doi:10.1016/j.tplants.2008.07.004
↑ Skylabs Inc. "Thiamine Hydrochloride Information." 2007.
↑ [1]
↑ Thiamine's Mood-Mending Qualities, Richard N. Podel, Nutrition Science News, January 1999.
↑ McGuire, M. and K.A. Beerman. Nutritional Sciences: From Fundamentals to Foods. 2007. California: Thomas Wadsworth.
↑ Hayes KC, Hegsted DM. Toxicity of the Vitamins. In: National Research Council (U.S.). Food Protection Committee. Toxicants Occurring Naturally in Foods. 2nd ed. Washington DCL: National Academy Press; 1973.
↑ Bettendorff L., Mastrogiacomo F., Kish S. J., and Grisar T. «Thiamine, thiamine phosphates and their metabolizing enzymes in human brain». J. Neurochem., 66, 1, 1996, pàg. 250–258. DOI: 10.1046/j.1471-4159.1996.66010250.x. PMID: 8522961.
↑ 22,022,122,222,3 Tanphaichitr V. Thiamin. In: Shils ME, Olsen JA, Shike M et al., editors. Modern Nutrition in Health and Disease. 9th ed. Baltimore: Lippincott Williams & Wilkins; 1999
↑ Butterworth RF. Thiamin. In: Shils ME, Shike M, Ross AC, Caballero B, Cousins RJ, editors. Modern Nutrition in Health and Disease, 10th ed. Baltimore: Lippincott Williams & Wilkins; 2006
↑ Makarchikov AF, Lakaye B, Gulyai IE, Czerniecki J, Coumans B, Wins P, Grisar T and Bettendorff L «Thiamine triphosphate and thiamine triphosphatase activities: from bacteria to mammals». Cell. Mol. Life Sci, 60, 7, 2003, pàg. 1477–1488. DOI: 10.1007/s00018-003-3098-4. PMID: 12943234.
↑ Lakaye B, Wirtzfeld B, Wins P, Grisar T and Bettendorff L «Thiamine triphosphate, a new signal required for optimal growth of Escherichia coli during amino acid starvation». J. Biol. Chem., 279, 17, 2004, pàg. 17142–17147. DOI: 10.1074/jbc.M313569200. PMID: 14769791.
↑ 26,026,126,2 Frédérich M., Delvaux D., Gigliobianco T., Gangolf M., Dive G., Mazzucchelli G., Elias B., De Pauw E., Angenot L., Wins P. and Bettendorff L. «Thiaminylated adenine nucleotides — chemical synthesis, structural characterization and natural occurrence FEBS J.». FEBS Journal, 276, 12, 2009, pàg. 3256–3268. DOI: 10.1111/j.1742-4658.2009.07040.x. PMID: 19438713.
↑ "Thiamin", Jane Higdon, Micronutrient Information Center, Linus Pauling Institute
↑ 28,028,128,228,328,4 Butterworth RF. Thiamin. In: Shils ME, Shike M, Ross AC, Caballero B, Cousins RJ, editors. Modern Nutrition in Health and Disease, 10th ed. Baltimore: Lippincott Williams & Wilkins; 2006.
↑ Thornalley PJ «The potential role of thiamine (vitamin B(1)) in diabetic complications». Curr Diabetes Rev, 1, 3, 2005, pàg. 287–98. DOI: 10.2174/157339905774574383. PMID: 18220605.
↑ Diabetes problems 'vitamin link', BBC News, Tuesday, 7 August 2007
↑ Maurice V, Adams RD, Collins GH. The Wernicke-Korsakoff Syndrome and Related Neurologic Disorders Due to Alcoholism and Malnutrition. 2nd ed. Philadelphia: FA Davis, 1989.
↑ Martin, PR, Singleton, CK, Hiller-Sturmhofel, S «The role of thiamine deficiency in alcoholic brain disease». Alcohol Research and Health, 27, 2, 2003, pàg. 134–142. PMID: 15303623.
↑ 33,033,1 Kril JJ «Neuropathology of thiamine deficiency disorders». Metab Brain Dis, 11, 1, 1996, pàg. 9–17. DOI: 10.1007/BF02080928. PMID: 8815394.
↑ Butterworth RF, Gaudreau C, Vincelette J et al. «Thiamine deficiency and wernicke's encephalopathy in AIDS». Metab Brain Dis, 6, 4, 1991, pàg. 207–12. DOI: 10.1007/BF00996920. PMID: 1812394.
↑ Harper C. «Wernicke’s encephalopathy, a more common disease than realised (a neuropathological study of 51 cases)». J Neurol Neurosurg Psychol, 42, 3, 1979, pàg. 226–231. DOI: 10.1136/jnnp.42.3.226. PMC: 490724. PMID: 438830.
↑ Butterworth RF «Pathophysiologic mechanisms responsible for the reversible (thiamine-responsive) and irreversible (thiamine non-responsive) neurological symptoms of Wernicke's encephalopathy». Drug Alcohol Rev, 12, 3, 1993, pàg. 315–22. DOI: 10.1080/09595239300185371. PMID: 16840290.
↑ Rindi G, Imarisio L, Patrini C «Effects of acute and chronic ethanol administration on regional thiamin pyrophosphokinase activity of the rat brain». Biochem Pharmacol, 35, 22, 1986, pàg. 3903–8. DOI: 10.1016/0006-2952(86)90002-X. PMID: 3022743.
↑ McCollum EV A History of Nutrition. Cambridge, MA: Riverside Press, Houghton Mifflin; 1957.
↑ Merck Veterinary Manual, ed 1967, pp 1440-1441.
↑ R.E. Austic and M.L. Scott, Nutritional deficiency diseases, in Diseases of poultry, ed. by M.S. Hofstad, Iowa State University Press, Ames, Iowa, USA ISBN 0-8138-0430-2, p. 50.
↑ The disease is described more carefully here: merckvetmanual.com
↑ National Research Council. 1996. Nutrient Requirements of Beef Cattle, Seventh Revised Ed. Washington, D.C.: National Academy Press.
↑ Polioencephalomalacia: Introduction, Merck Veterinary Manual
↑ Polioencephalomacia: Introduction, "ACES Publications"
↑ 45,045,1 Balk L, Hägerroth PA, Akerman G, Hanson M, Tjärnlund U, Hansson T, Hallgrimsson GT, Zebühr Y, Broman D, Mörner T, Sundberg H. (2009). Wild birds of declining European species are dying from a thiamine deficiency syndrome. Proc Natl Acad Sci U S A. 106:12001–12006. PMID: 19597145 doi:10.1073/pnas.0902903106
↑ Bettendorff L, Peeters M., Jouan C., Wins P., and Schoffeniels E. (1991) Determination of thiamin and its phosphate esters in cultured neurons and astrocytes using an ion-pair reversed-phase high-performance liquid chromatographic method. Anal. Biochem. 198: 52-59.
↑ Losa R, Sierra MI, Fernández A, Blanco D, Buesa JM. (2005) Determination of thiamine and its phosphorylated forms in human plasma, erythrocytes and urine by HPLC and fluorescence detection: a preliminary study on cancer patients.J Pharm Biomed Anal. 37:1025-1029.
↑ Lu J, Frank EL. (2008) Rapid HPLC measurement of thiamine and its phosphate esters in whole blood. Clin Chem. 2008 May;54(5):901-906.
↑ Shabangi M, Sutton JA. Separation of thiamin and its phosphate esters by capillary zone electrophoresis and its application to the analysis of water-soluble vitamins. Journal of Pharmaceutical and Biomedical Analysis 2005; 38:1:66-71.
↑ Slater, PV «Thiamine Responsive Megaloblastic Anemia with severe diabetes mellitus and sensorineural deafness (TRMA)». The Australian nurses' journal, 7, 11, 1978, pàg. 40–3. PMID: 249270.
↑ Kopriva, V; Bilkovic, R; Licko, T «Tumours of the small intestine (author's transl)». Ceskoslovenska gastroenterologie a vyziva, 31, 8, Dec 1977, pàg. 549–53. ISSN: 0009-0565. PMID: 603941.
↑ Beissel, J «The role of right catheterization in valvular prosthesis surveillance (author's transl)». Annales de cardiologie et d'angeiologie, 26, 6, Dec 1977, pàg. 587–9. ISSN: 0003-3928. PMID: 606152.
↑ Mendelian Inheritance in Man (OMIM) 249270
↑ Butterworth RF. Pyruvate dehydrogenase deficiency disorders. In: McCandless DW, ed. Cerebral Energy Metabolism and Metabolic Encephalopathy. Plenum Publishing Corp.; 1985.
↑ Blass JP. Inborn errors of pyruvate metabolism. In: Stanbury JB, Wyngaarden JB, Frederckson DS et al., eds. Metabolic Basis of Inherited Disease. 5th ed. New York: McGraw-Hill, 1983.
↑ Djoenaidi W, Notermans SL, Gabreëls-Festen AA, Lilisantoso AH, Sudanawidjaja A «Experimentally induced beriberi polyneuropathy in chickens». Electromyogr Clin Neurophysiol, 35, 1, 1995, pàg. 53–60. PMID: 7737017.
↑ Bruce WR, Furrer R, Shangari N, O’Brien PJ, Medline A, Wang Y «Marginal dietary thiamin deficiency induces the formation of colonic aberrant crypt foci (ACF) in rats». Cancer Lett, 202, 2, 2003, pàg. 125–129. DOI: 10.1016/j.canlet.2003.08.005. PMID: 14643441.
↑ Langlais PJ «Pathogenesis of diencephalic lesions in an experimental model of Wernicke's encephalopathy». Metab Brain Dis, 10, 1, 1995, pàg. 31–44. DOI: 10.1007/BF01991781. PMID: 7596327.
↑ Frederikse PH, Zigler SJ Jr, Farnsworth PN, Carper DA «Prion protein expression in mammalian lenses». Curr Eye Res, 20, 2, 2000, pàg. 137–43. DOI: 10.1076/0271-3683(200002)20:2;1-D;FT137. PMID: 10617916.
↑ Kale S, Ulas G, Song J, Brudvig GW, Furey W & Jordan F (2008) Efficient coupling of catalysis and dynamics in the E1 component of Escherichia coli pyruvate dehydrogenase multienzyme complex.Proc Natl Acad Sci U S A. 105, 1158-1163
↑ Kluger R & Tittmann K (2008) Thiamin diphosphate catalysis: enzymic and nonenzymic covalent intermediates. Chem Rev 108, 1797-1833
↑ Makarchikov AF, Lakaye B, Gulyai IE, Czerniecki J, Coumans B, Wins P, Grisar T & Bettendorff L (2003) Thiamine triphosphate and thiamine triphosphatase activities: from bacteria to mammals. Cell Mol Life Sci 60, 1477-1488.
↑ Bettendorff L. and Wins P. «Thiamin diphosphate in biological chemistry : new aspects of thiamin metabolism, especially triphosphate derivatives acting other than as cofactors». FEBS J., 276, 11, 2009, pàg. 2917–2925. DOI: 10.1111/j.1742-4658.2009.07017.x. PMID: 19490098.
Enllaços externs
| A Wikimedia Commons hi ha contingut multimèdia relatiu a: Tiamina |
"Branched-Chain Amino Acid Metabolism" at ncbi.nlm.nih.gov (en anglès)
Thiamin deficiency in poultry (en anglès)
Type of vitamin B1 could treat common cause of blindness (en anglès)