Cromat
| Substància | oxoanió |
|---|---|
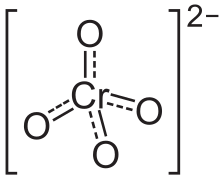
| Estructura química | |
| Fórmula química | CrO₄²⁻ |
 | |

Mostra de cromat de potassi.
Els cromats i els dicromats són sals de l'àcid cròmic i de l'àcid dicròmic, respectivament. Els cromats contenen l'ió CrO42−, que els dóna un fort color groc.[1] Els dicromats tenen l'ió Cr2O72−, pel que són d'un color ataronjat intens.[2] Els àtoms de crom es troben en estat d'oxidació +6 en ambdós, el que fa que aquests compostos siguin en general forts oxidants. En solució aquosa, el cromat i el dicromat es troben en equilibri.

Mostra de dicromat de potassi.
- CrO42− + 2 H3O+ ⇌ Cr2O72− + 3 H2O
En baixar el pH de la solució, predomina l'ió dicromat, mentre el cromat predomina en un pH més alt. Això és un clàssic exemple del Principi de Le Châtelier. La concentració de cromat també afecta a l'equilibri.
- Són usats en anàlisi ambiental per mesurar la demanda química d'oxigen (DQO).
- Són cancerígens. Tots els composts amb crom en estat d'oxidació 6+ són considerats tòxics i cancerígens.
- En ser usats com valorants en una reacció d'oxidoreducció, són reduïts a crom (III), Cr3+, d'un color blau-verdós.
- Les sals de sodi (Na+), potassi (K+), i amoni (NH4+) són sòlids cristal·lins solubles en aigua i són els cromats i dicromats més comunament usats com a reactius. En general, els cromats i dicromats de metalls pesants són poc o gens solubles en aigua per la qual cosa no tenen utilitat com reactius.
Estructures
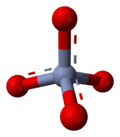 |  | 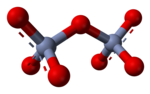 |  |
| Estructura tetraèdrica de l'ió cromat. CrO42− | L'ió dicromat, Cr2O72−, consisteix en dos tetràedres units a un àtom d'oxigen. | ||
Referències
↑ «Cromat». l'Enciclopèdia. [Consulta: 9 maig 2010].
↑ «Dicromat». l'Enciclopèdia. [Consulta: 9 maig 2010].
Enllaços externs
| A Wikimedia Commons hi ha contingut multimèdia relatiu a: Cromat |
- Crom
Com afecten els canvis de concentració l'equilibri químic? PDF
PDF